医疗器械唯一标识数据库填报指南
前言
本标准按照GB/T 1.1—2009给出的规则起草。
请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别这些专利的责任。
本标准由国家药品监督管理局提出。
本标准由国家药品监督管理局信息中心归口。
本标准起草单位:国家药品监督管理局信息中心、中国标准化研究院、中国人民解放军总医院。
本标准主要起草人:陈锋、郭媛媛、张原、何昆仑、刘靓、张文思、李丹丹、李强、刘鹏。
1 范围
本标准规定了向医疗器械唯一标识数据库(简称数据库)填报产品标识及其相关信息的基本要求。
本标准适用于医疗器械唯一标识数据库的填报。
2 规范性引用文件
下列文件对于本文件的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
YY/T 1752—2020 医疗器械唯一标识数据库基本数据集
3 术语和定义
YY/T 1752—2020界定的以及下列术语和定义适用于本文件。
3.1 数据接口 data interface
计算机软件系统之间传递数据、交换信息的接口,以电子文件的形式实现。
4 缩略语
下列缩略语适用于本文件。
XML:可扩展标记语言(Extensible Markup Language)
JSON:JavaScript对象表示法(JavaScript Object Notation)
5 数据填报方式
可采用网页填报、数据模板导入和数据接口交换3种方式填报。
当采用网页填报方式时,按照网页填报提示填报相关数据。数据填报内容参见附录A。
当采用数据模板导入方式时,应按照医疗器械唯一标识数据库提供的数据模板填写数据,数据格式和内容应符合数据模板的相关要求,之后导入数据库。数据填报内容参见附录A。
当采用数据接口交换方式时,应开发数据交互接口,在通过数据库对接服务注册后,可与数据库建立数据交换关系。数据接口交换格式可采用XML、JSON两种格式,格式示例参见附录B。
6 数据接口交换格式要求
6.1 XML 格式
使用XML格式传输数据库基本信息数据子集对应的数据记录时,应将数据记录描述为udid元素,udid元素的XML格式规则如图1所示,具体描述参见B.1,其中:
datasetName元素:数据记录名称;
dataset元素:基本信息列表元素,包含一条或多条data元素;
data元素:包含一条数据记录中的所有内容,由多个数据项和数据项值构成;
uploadType元素:数据申报类型,add为新增,modify为修改编辑,用于标识区分业务操作类型;
deviceRecordKey元素:数据库生成的唯一的最小销售单元产品标识记录编码,当数据申报类型为modify修改编辑时,该字段必填;
devicePackage元素:包装产品标识信息列表元素,包含0条或多条packing元素;
packing元素:包装产品标识信息元素;
deviceStorage元素:医疗器械储存或操作条件信息列表元素,包含0条或多条storage元素;
storage元素:储存或操作条件信息元素;
deviceClinical元素:医疗器械临床使用尺寸信息列表元素,包含0条或多条clinical元素;
clinical元素:临床使用尺寸信息元素。



6.2 JSON 格式
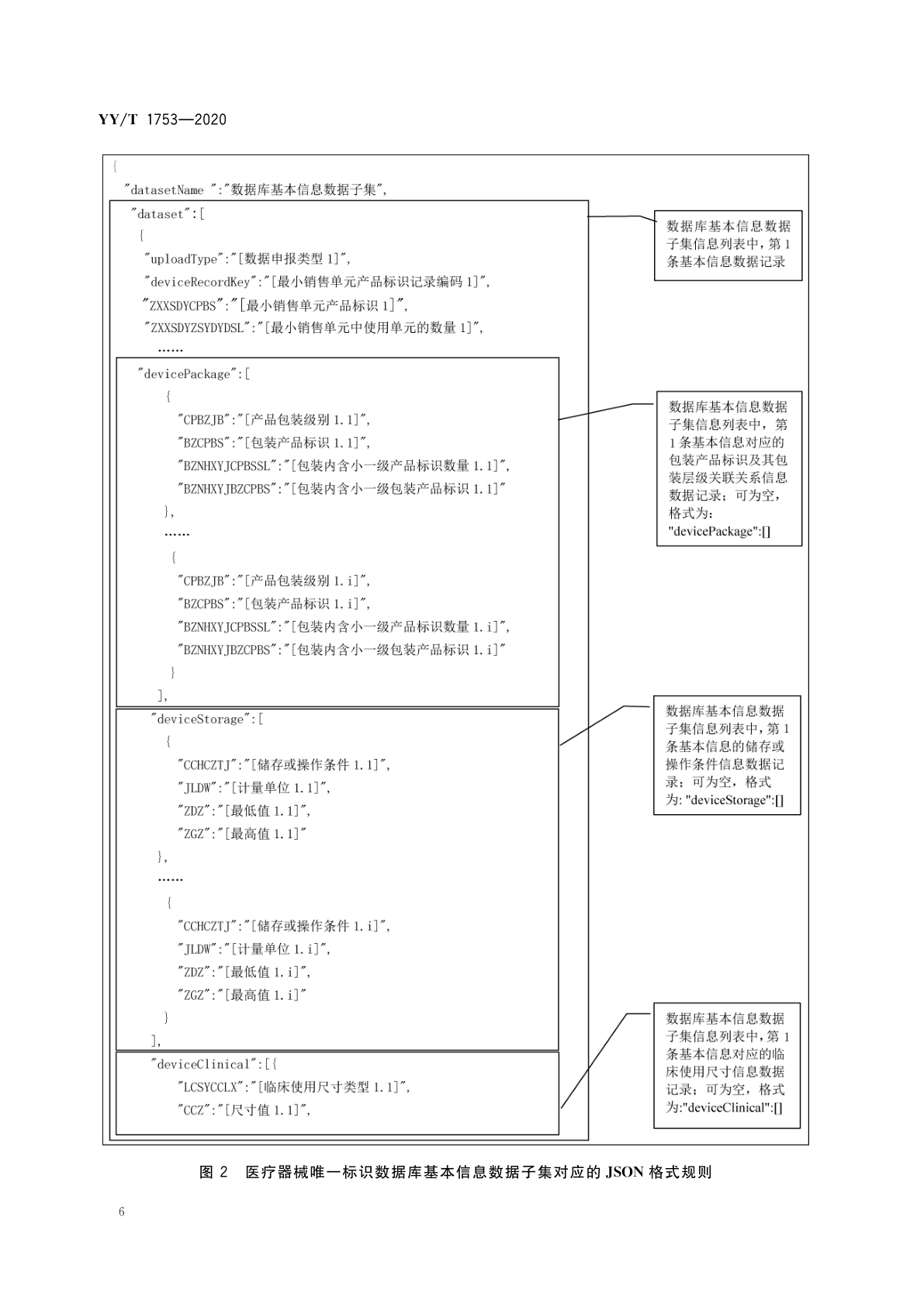
使用JSON格式传输数据库基本信息数据子集对应的数据记录时,应将数据记录描述为dataset数组,dataset数组的JSON格式规则如图2所示,具体描述参见附录B.2,其中:
datasetName对象:数据记录名称;
dataset数组:数据库基本信息数据子集列表数组,包含一条或多条数组;
uploadType对象:数据申报类型,add为新增,modify为修改编辑,用于标识区分业务操作类型;
deviceRecordKey对象:数据库生成的唯一的最小销售单元产品标识记录编码,当数据申报类型为modify修改编辑时,该字段必填;
devicePackage数组:包装产品标识信息列表数组,包含0条或多条包装产品标识信息;
deviceStorage数组:医疗器械储存或操作条件信息列表数组,包含0条或多条储存或操作条件信息;
deviceClinical数组:医疗器械临床使用尺寸信息列表数组,包含0条或多条clinical数组。


7 数据填报内容
医疗器械唯一标识数据库数据填报内容应包括YY/T 1752—2020中7.1的内容。
8 数据填报安全要求
8.1 接入认证
在进行数据传输时,数据库应对填报人进行身份认证,并验证相应请求权限。
8.2 数据加密
在进行数据交换时,如涉及敏感信息应按照数据库相关要求进行数据加密。
8.3 传输安全
数据传输应使用安全的传输协议。
8.4 消息状态回执
在进行数据交换时,数据库应向填报人返回包含处理结果的消息状态回执。
8.5 日志记录
数据库应对数据接口调用请求进行记录及异常警告。
附录A(资料性附录)
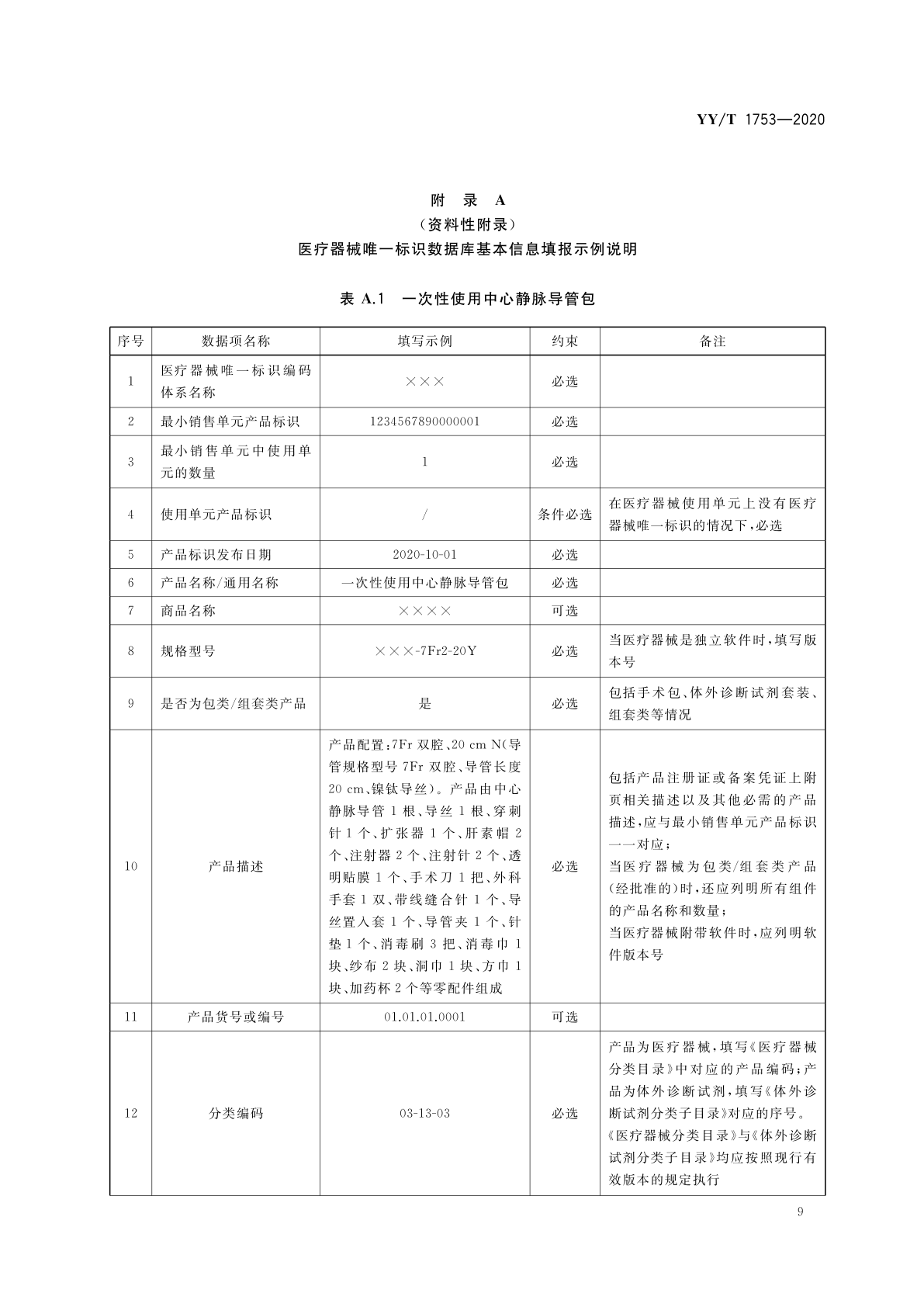
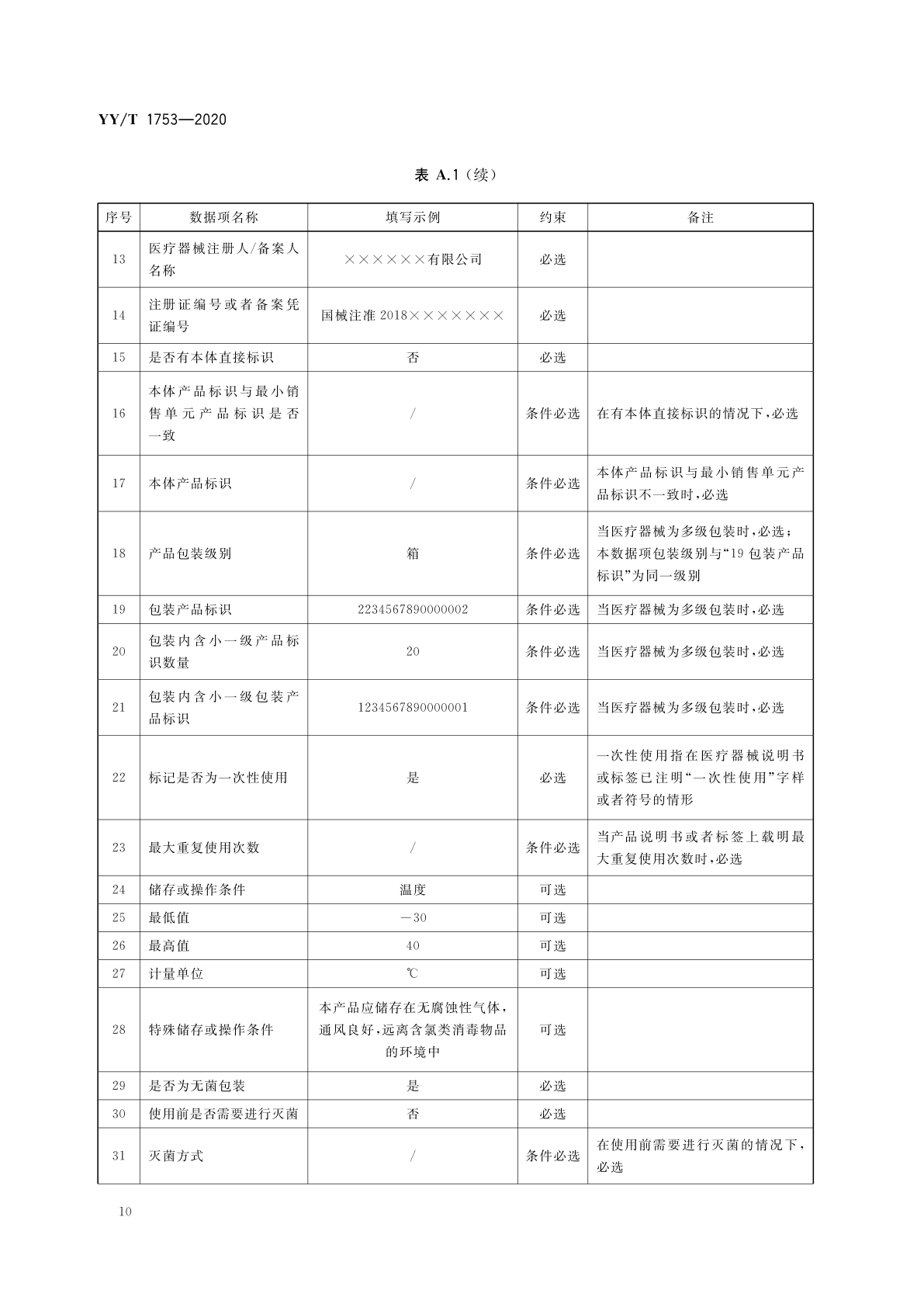
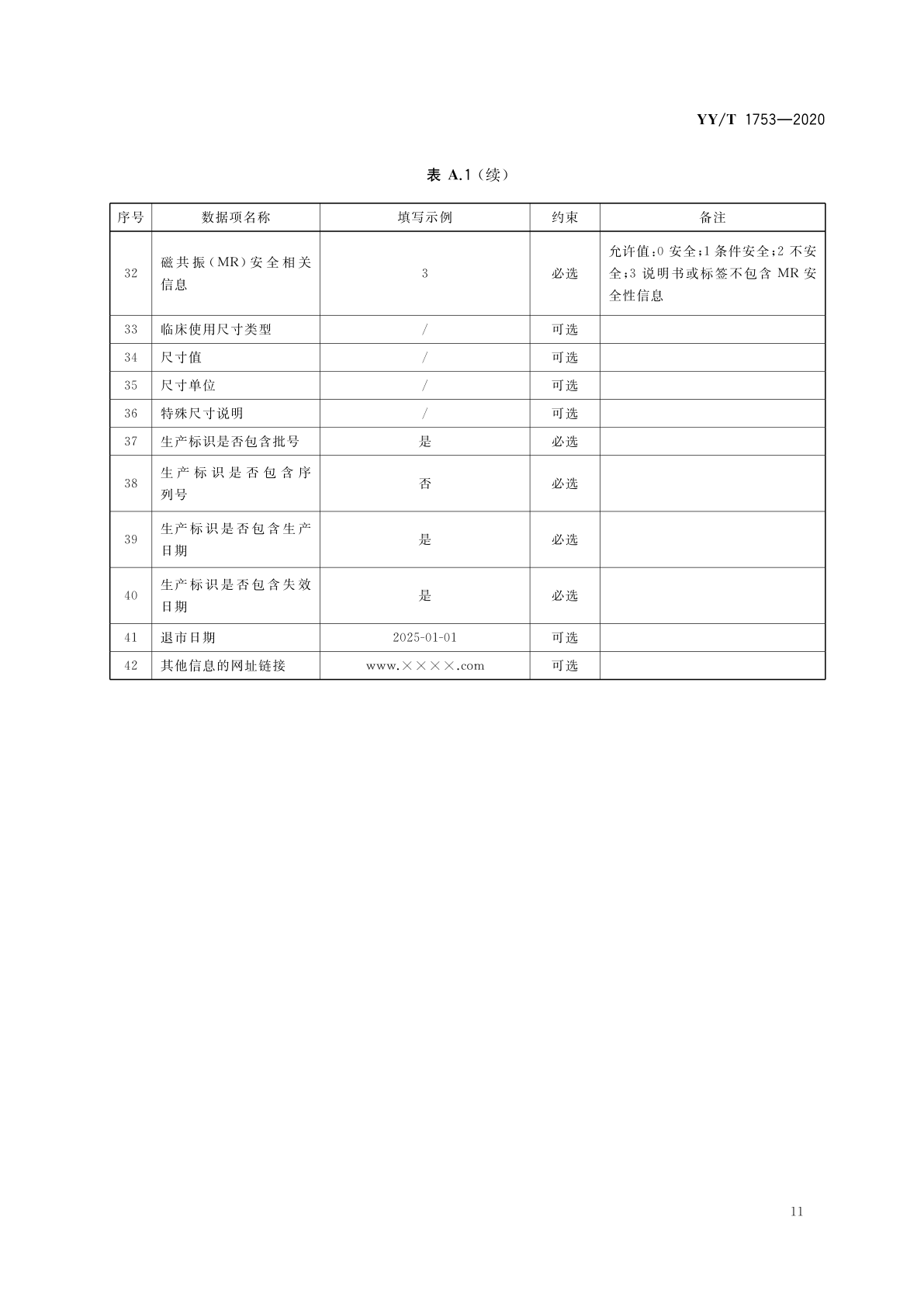
医疗器械唯一标识数据库基本信息填报示例说明
表A.1 一次性使用中心静脉导管包:
附录B(资料性附录)
医疗器械唯一标识数据库数据填报接口格式示例
B.1 医疗器械唯一标识数据库基本信息的XML格式示例

B.2 医疗器械唯一标识数据库基本信息的JSON格式示例

参考文献
[1] 国家药监局关于发布医疗器械唯一标识系统规则的公告(2019年第66号)
[2] Food and Drug Administration. GUDID-Data-Elements-Reference-Table [EB/OL]
附件: