医疗器械唯一标识应用技术规范
前言
本文件按照GB/T 1.1—2020《标准化工作导则 第1部分:标准化文件的结构和起草规则》的规定起草。
请注意本文件的某些内容可能涉及专利。本文件的发布机构不承担识别专利的责任。
本文件由威海市市场监督管理局提出、归口并组织实施和评估。
本文件起草单位:威海市产品质量标准计量检验研究院、威海市市场监督管理局、禾木(中国)生物工程有限公司、威海市工业和信息化发展中心、威海市食品药品检验检测研究院。
本文件主要起草人:王艳华、刘晓、李琳、林宇春、王吉成、宫汝燕、才洪冰、李钰、孙佳敏、冯建岭、孔令涛、刘超、齐凯、潘盛南、周青。
1 范围
本文件规定了医疗器械唯一标识应用的缩略语、应用技术要求。
本文件适用于基于GS1标准的医疗器械唯一标识的实施应用。
2 规范性引用文件
下列文件中的内容通过文中的规范性引用而构成本文件必不可少的条款。其中,注日期的引用文件,仅该日期对应的版本适用于本文件;不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。
GB 12904-2008 商品条码 零售商品编码与条码表示
GB/T 16830-2008 商品条码 储运包装商品编码与条码表示
GB/T 16986-2018 商品条码 应用标识符
YY/T 1681 医疗器械唯一标识系统基础术语
YY/T 1879 医疗器械唯一标识的创建和赋予
3 术语和定义
YY/T 1681界定的以及下列术语和定义适用于本文件。
3.1 医疗器械唯一标识 unique device identifier;UDI
基于标准创建的一系列由数字、字母和/或符号组成的代码,包括产品标识和生产标识,用于对医疗器械进行唯一性识别。
注1:“唯一”一词并不意味着对单个产品进行序列化管理。
注2:可用于医疗器械产品的管理和追溯等。
[来源:YY/T 1681—2019,3.1]
3.2 产品标识 device identifier;UDI-DI
特定于某种规格型号和包装医疗器械的唯一性代码。
注:产品标识可用作对医疗器械唯一标识数据库存储信息的“访问关键字”,关联医疗器械产品信息、制造商信息、注册信息等。
[来源:YY/T 1681—2019,3.2]
3.3 生产标识 production identifier;UDI-PI
识别医疗器械生产过程相关数据的代码。
注:根据实际应用需求,生产标识可包含医疗器械序列号、生产批号、生产日期、失效日期等。
[来源:YY/T 1681—2019,3.3]
3.4 应用标识符 application identifier;AI
标识数据含义与格式的字符,由2位~4位数字组成。
[来源:GB/T 16986—2018,3.1]
4 缩略语
下列缩略语适用于本文件。
UDI:医疗器械唯一标识(unique device identifier)
UDI-DI:医疗器械产品标识(device identifier)
UDI-PI:医疗器械生产标识(production identifier)
AI:应用标识符(application identifier)
GS1:国际物品编码协会(global standard 1)
GTIN:全球贸易项目代码(global trade item number)
RFID:射频识别(radio frequency identification)
5 应用技术要求
5.1 申请厂商识别代码
5.1.1 厂商识别代码是基于GS1标准的UDI的重要组成部分。
5.1.2 厂商识别代码由7位~10位数字组成。
5.1.3 厂商识别代码由中国物品编码中心负责分配和管理,企业宜通过中国物品编码中心官网或咨询市场监督管理部门提交资料申请和办理。
5.2 分配 UDI 编码标识
5.2.1 分配 UDI-DI
5.2.1.1 代码结构
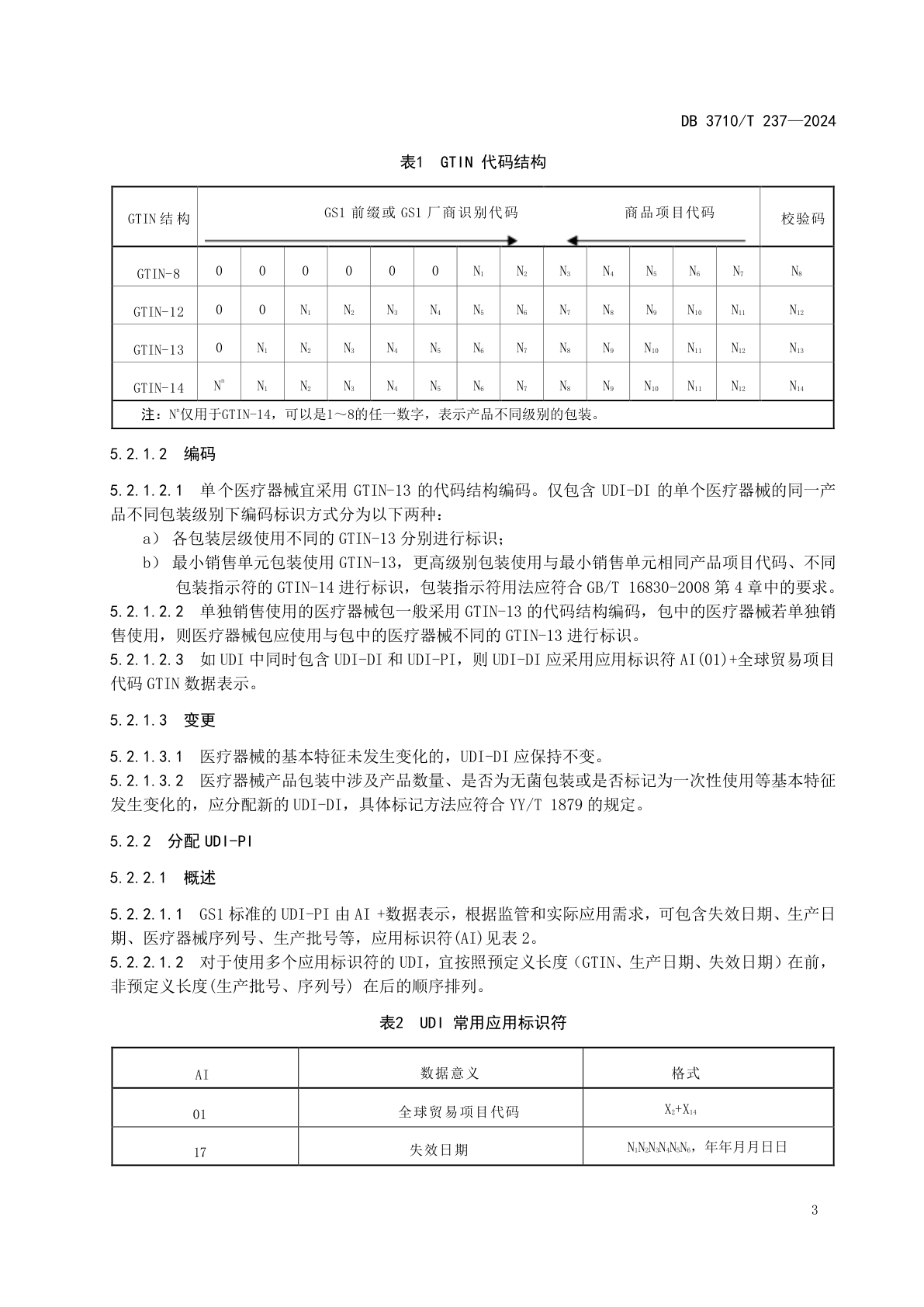
5.2.1.1.1 GS1标准的UDI-DI采用GTIN进行标识,由GS1厂商识别代码、商品项目代码和校验码组成,共有GTIN-8、GTIN-12、GTIN-13和GTIN-14四种结构,见表1。
5.2.1.1.2 商品项目代码由2位~5位数字组成,相应编码要求应符合GB 12904的要求。
5.2.1.1.3 校验码为1位数字,用于检验译码正确性,算法应按照GB 12904-2008中附录B的计算方法进行。
5.2.1.1.4 所有结构的GTIN在数据库存储时均应为14位数据字符串,长度小于14位的GTIN应在开头填充零作为补位。
表1:
5.2.1.2 编码
5.2.1.2.1 单个医疗器械宜采用GTIN-13的代码结构编码。仅包含UDI-DI的单个医疗器械的同一产品不同包装级别下编码标识方式分为以下两种:
a)各包装层级使用不同的GTIN-13分别进行标识;
b)最小销售单元包装使用GTIN-13,更高级别包装使用与最小销售单元相同产品项目代码、不同包装指示符的GTIN-14进行标识,包装指示符用法应符合GB/T 16830-2008第4章中的要求。
5.2.1.2.2 单独销售使用的医疗器械包一般采用GTIN-13的代码结构编码,包中的医疗器械若单独销售使用,则医疗器械包应使用与包中的医疗器械不同的GTIN-13进行标识。
5.2.1.2.3 如UDI中同时包含UDI-DI和UDI-PI,则UDI-DI应采用应用标识符AI(01)+全球贸易项目代码GTIN数据表示。
5.2.1.3 变更
5.2.1.3.1 医疗器械的基本特征未发生变化的,UDI-DI应保持不变。
5.2.1.3.2 医疗器械产品包装中涉及产品数量、是否为无菌包装或是否标记为一次性使用等基本特征发生变化的,应分配新的UDI-DI,具体标记方法应符合YY/T 1879的规定。
5.2.2 分配 UDI-PI
5.2.2.1 概述
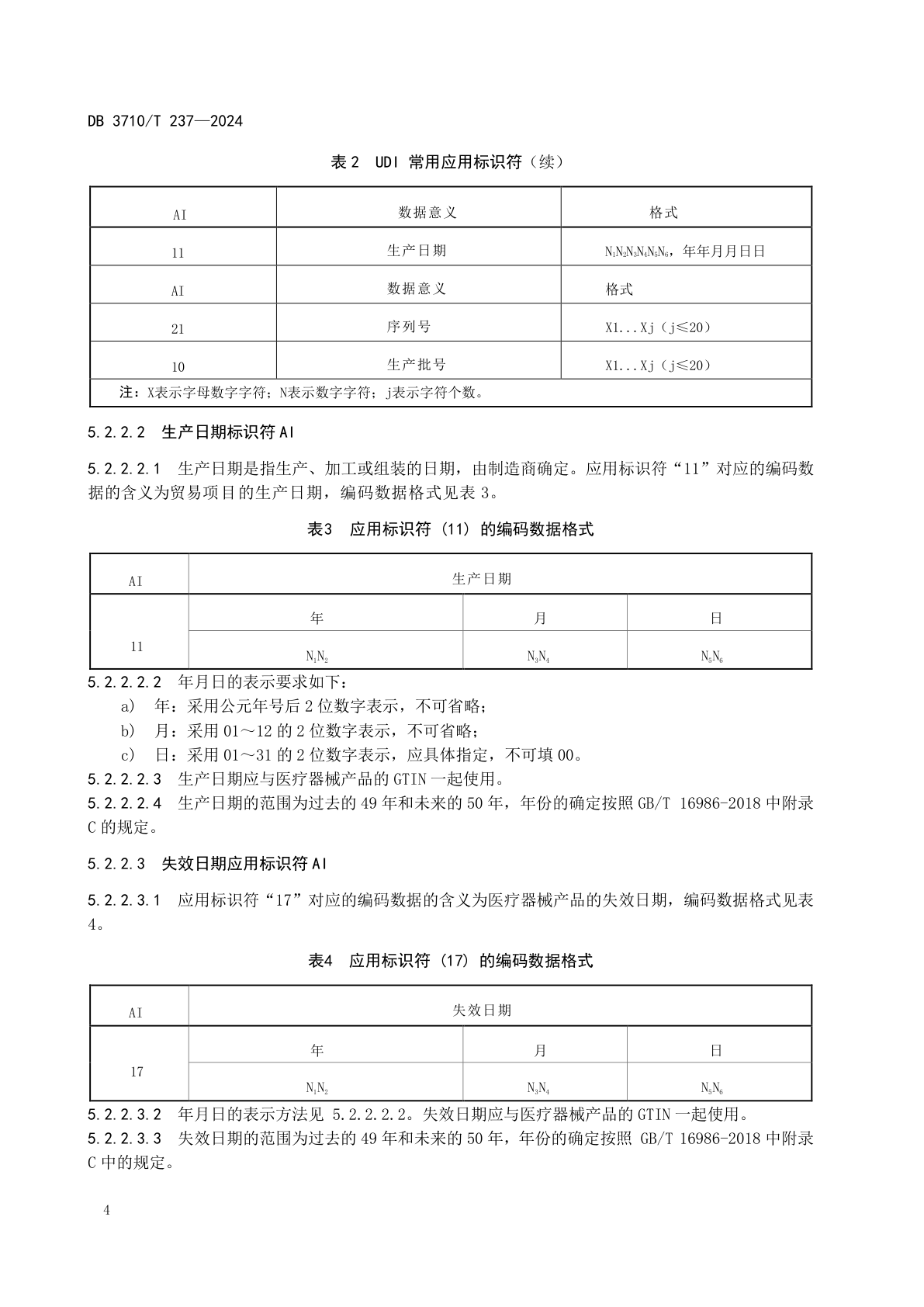
5.2.2.1.1 GS1标准的UDI-PI由AI + 数据表示,根据监管和实际应用需求,可包含失效日期、生产日期、医疗器械序列号、生产批号等,应用标识符(AI)见表2。
5.2.2.1.2 对于使用多个应用标识符的UDI,宜按照预定义长度(GTIN、生产日期、失效日期)在前,非预定义长度(生产批号、序列号)在后的顺序排列。
表2至表4:
5.2.2.2 生产日期标识符 AI
5.2.2.2.1 生产日期是指生产、加工或组装的日期,由制造商确定。应用标识符“11”对应的编码数据的含义为贸易项目的生产日期。
5.2.2.2.2 年月日的表示要求如下:
a)年:采用公元年号后2位数字表示,不可省略;
b)月:采用01~12的2位数字表示,不可省略;
c)日:采用01~31的2位数字表示,应具体指定,不可填00。
5.2.2.2.3 生产日期应与医疗器械产品的GTIN一起使用。
5.2.2.2.4 生产日期的范围为过去的49年和未来的50年,年份的确定按照GB/T 16986-2018中附录C的规定。
5.2.2.3 失效日期应用标识符 AI
5.2.2.3.1 应用标识符“17”对应的编码数据的含义为医疗器械产品的失效日期。
5.2.2.3.2 年月日的表示方法见 5.2.2.2.2。失效日期应与医疗器械产品的GTIN一起使用。
5.2.2.3.3 失效日期的范围为过去的49年和未来的50年,年份的确定按照GB/T 16986-2018中附录C中的规定。
5.2.2.4 生产批号应用标识符 AI
5.2.2.4.1 应用标识符“10”对应的编码数据的含义为医疗器械产品的生产批号代码。
5.2.2.4.2 生产批号是与医疗器械产品相关的数据信息,用于产品追溯。
5.2.2.4.3 生产批号数据信息可涉及医疗器械产品本身或其所包含的项目。
注:包括产品的组号、班次号、机器号、时间或内部的产品代码等。
5.2.2.4.4 生产批号为字母数字字符,长度可变,最长20位,其字符按照GB/T 16986-2018中附录D的规定。
5.2.2.4.5 生产批号应与医疗器械产品的GTIN一起使用。
5.2.2.5 序列号应用标识符 AI
5.2.2.5.1 应用标识符“21”对应的编码数据的含义为医疗器械产品的序列号。
5.2.2.5.2 序列号是分配给实体的与GTIN结合对每个产品进行唯一标识的一种永久性的系列代码。
5.2.2.5.3 序列号由制造商分配,为字母数字字符,长度可变,最长20位,其字符按照GB/T 16986-2018中附录B的规定。
5.2.2.5.4 序列号应与医疗器械产品的GTIN一起使用。
表5、表6及图1:

5.3 UDI 数据载体
GS1标准的UDI数据载体可采用三种形式,企业可根据实际情况组合采用,分别是一维码(EAN-13、GS1-128、ITF-14、GS1 DataBar)、二维码(GS1 DataMatrix)和射频识别(RFID),常见UDI载体示例见图1至图8,ITF-14示例见GB/T 16830-2008附录B和附录C。


5.4 数据发布及更新
5.4.1 登录国家医疗器械监管部门医疗器械唯一标识数据库,在医疗器械监管部门UDI数据库中按照逐个录入、批量导入和接口对接三种方式上传产品UDI信息,核准无误后发布。
5.4.2 当医疗器械的UDI数据发生变化时,应于产品上市销售前及时在医疗器械唯一标识数据库中进行变更,实现数据的同步更新。
附件: